EXAMEN ADMISION UNI RESUELTO DE QUIMICA INGRESO UNIVERSIDAD DE INGENIERÍA PDF
PREGUNTA 1 :
Respecto a la teoría mecano-cuántica y la estructura atómica, ¿cuáles de las siguientes proposiciones son correctas?
I. El electrón ya no están en una órbita, en el sentido de Bohr, sino más bien hay una nube de probabilidad electrónica.
II. Cada uno de los estados cuánticos, diferenciados por n, l, ml, corresponde a distintas funciones de distribución de probabilidad (orbitales).
III. La función de probabilidad más sencilla se obtiene para los estado s (l=10) y tienen simetría esférica.
A) solo I
B) solo III
C) I y II
D) II y III
E) I, II y III
RESOLUCIÓN :
Tema: Modelo atómico del átomo
I. Correcta
Según el principio de incertidumbre de Heisenberg, es imposible determinar simultáneamente y con exactitud la posición y la velocidad de un electrón; por ello se descarta la órbita circular propuesta por Bohr y se incluye el concepto de orbital o nube electrónica como la región donde es más probable encontrar al electrón.
II. Correcta
Un orbital o función de onda se describe por los tres primeros números cuánticos (n, l, ml), los cuales derivan de la solución de la ecuación de onda de Schrödinger.
n: indica el tamaño del orbital.
l: indica la forma del orbital.
ml: indica la orientación espacial del orbital.
III. Correcta
El orbital Sharp o s (l=0) tiene forma esférica y es el orbital de mayor simetría.
Rpta. : "E"
PREGUNTA 2 :
La corrosión de un metal es un proceso espontáneo a temperatura ambiente. Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I. La corrosión implica un proceso de oxidación reducción.
II. En algunos casos, la corrosión del metal forma una capa protectora que disminuye el proceso de corrosión.
III. El daño estructural por efectos de la corrosión tiene una alta repercusión económica.
A) solo I
B) I y III
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
TEMA : Electroquímica
La corrosión se define como el deterioro de un material a consecuencia de un ataque electroquímico por parte de su entorno. De manera más general, puede entenderse como la tendencia general que tienen los materiales a buscar su forma más estable.
La velocidad a la que tiene lugar la corrosión dependerá en alguna medida de la temperatura y la salinidad, y de la concentración del fluido en contacto con el metal.
En la corrosión de algunos metales, como es el caso del aluminio, se forma una capa de óxido muy fina que impide el contacto entre el oxígeno del aire y el aluminio, por lo que podemos considerar la formación de una capa protectora que disminuye el proceso de corrosión.
I. Correcta
En la corrosión del hierro, el hierro se oxida y el oxígeno del aire se reduce.
II. Correcta
En la corrosión del aluminio se forma el Al2O3 que actúa como una capa de pintura protegiendo al aluminio de la corrosión.
III. Correcta
Los costos de la corrosión implican la prevención como las técnicas de protección, el reemplazo de materiales, etc.
Rpta. : "E"
PREGUNTA 3 :
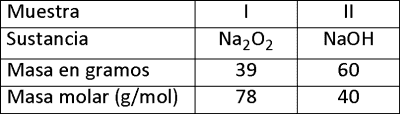
Dada la siguiente información:
Señale la alternativa correcta.
A) La muestra I corresponde a 1,5 mol de Na2O2.
B) La muestra II corresponde a 0,5 mol de NaOH.
C) Ambas muestras presentan igual número de moles.
D) La muestra I presenta mayor número de moles que la muestra II.
E) La muestra II presenta mayor número de moles que la muestra I.
RESOLUCIÓN :
PREGUNTA 5 :
A) 20
B) 38
C) 65
D) 80
E) 90
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 6 :
A continuación se presenta un diagrama de fases genérico. ¿En qué puntos, de los señalados, se observarán 2 fases?
A) I, III y V
B) II y IV
C) III y V
D) I y IV
E) I y III
RESOLUCIÓN :
Rpta. : "A"
PREGUNTA 7 :
¿Cuántos de los siguientes fenómenos presentados en las proposiciones son químicos?
I. Laminación del cobre
II. Oxidación del hierro
III. Evaporación del agua
IV. Fermentación de la uva
V. Disolución del azúcar en agua
A) 1
B) 2
C) 3
D) 4
E) 5
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 8 :
Dados los siguientes procesos:
Indique la proposición correcta:
A) La primera energía de ionización del cloro corresponde a un proceso exotérmico.
B) La segunda energía de ionización del cloro es menor que la primera.
C) Es más fácil que el cloro pierda electrones que los gane.
D) La primera afinidad electrónica del cloro corresponde a un fenómeno endotérmico.
E) El ion Cl (g)− es más estable que el átomo de Cl(g).
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 9 :
La sanguina seca (pintura roja) contiene, como pigmento, aproximadamente el 63 % en masa de óxido férrico, ¿cuántos mililitros de ácido clorhídrico 2 M se requieren para que todo el pigmento contenido en 10 g de sanguina reacciones totalmente con el ácido?
A) 20
B) 40
C) 79
D) 118
E) 137
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 10 :
¿Cuántos gramos de sulfato de cobre pentahidrato, CuSO4 · 5H2O, serán necesarios para preparar 250 mL de una solución 0,1 M de CuSO4?
Masa atómica: Cu=63,5; S=32; O=16; H=1
A) 3,99
B) 5,12
C) 6,24
D) 8,75
E) 10,23
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 11 :
Los elementos del grupo 17 de la tabla periódica moderna son conocidos como halógenos (“formadores de sales”). ¿Cuál de los siguientes compuestos corresponde a una sal de un halógeno?
A) NH4NO3
B) K2S
C) NaCl
D) Mg3N2
E) Br2
RESOLUCIÓN :
Los elementos del grupo 17 o VIIA son conocidos como halógenos (F, Cl, Br, I) porque tienen la capacidad para formar sales.
Analizamos las alternativas propuestas.
A) No corresponde.
El NH4NO3 es un oxisal que no contiene un halógeno.
B) No corresponde
El K2S es una sal haloidea, pero no contiene un halógeno.
C) Sí corresponde
El NaCl es una sal que contiene al cloro, que es un halógeno.
D) No corresponde
El Mg3N2 es una sal haloidea que no contiene un halógeno.
E) No corresponde
El Br2 es una sustancia simple.
Rpta. : "C"
PREGUNTA 12 :
Una de las preocupaciones a nivel mundial es el calentamiento global originado por las actividades del hombre. Al respecto, señale la alternativa que presenta la secuencia correcta después de determinar si las proposiciones son verdaderas (V) o falsas (F).
I. El calentamiento global es consecuencia del aumento de la temperatura en la atmósfera terrestre.
II. El cambio climático que ocurre en la Tierra está relacionado principalmente al impacto de los gases de efecto invernadero.
III. El término efecto invernadero se refiere a la retención del calor en la atmósfera por parte de una capa de gases en la atmósfera, como por ejemplo el dióxido de carbono, el vapor de agua y metano.
A) VVV
B) VFV
C) VFF
D) FFV
E) FFF
RESOLUCIÓN :
Analizamos las proposiciones
I. Verdadera
A mayor temperatura de la atmósfera del planeta, se origina calentamiento global.
II. Verdadera
Los gases de efecto invernadero incrementan la temperatura de la Tierra.
III. Verdadera
El CO2, CH4 y H2O retienen el calor que debió salir del planeta.
Rpta. : "A"
PREGUNTA 13 :
A 25 ºC, el agua de lluvia puede llegar a tener un pOH de hasta 12. En este caso, ¿cuántas veces mayor es la concentración de iones hidronio de esta agua con respecto al agua neutra?
A) 12/7
B) 2/7
C) 5
D) 10^5
E) 10^12
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 14 :
Respecto al recurso agua, ¿cuáles de las siguientes proposiciones son correctas?
I. El agua nunca se encuentra pura en la naturaleza, debido a la facultad que tiene para disolver o dispersar diferentes sustancias.
II. El agua de lluvia recolectada, en la azotea de una vivienda, en un recipiente esterilizado, es agua pura.
III. La contaminación de las aguas con materia orgánica biodegradable disminuye la concentración de oxígeno disuelto.
A) solo I
B) solo II
C) solo III
D) I y III
E) I, II y III
RESOLUCIÓN :
TEMA : Contaminación ambiental
I. Correcta
El agua al tener la facultad de ser disolvente dispersa, por lo general, la mayor cantidad de sustancias, es por ello que no se le encuentra en la naturaleza en estado puro.
II. Incorrecta
El agua de lluvia, al precipitar, se mezcla en el camino con muchos componentes gaseosos y no gaseosos tales como CO2, SO2, polvo, hidrocarburos provenientes de incineraciones, quema de combustibles, entre otros; por consiguientes, no es pura.
III. Correcta
En la descomposición de la materia orgánica biodegradable, las bacterias consumen el oxígeno disuelto, reduciendo su concentración y afectando la vida de los peces.
Rpta. : "D"
PREGUNTA 15 :
Una posible solución a la contaminación relacionada a los gases emanados por los motores de los autos es el uso de celdas de combustible H2-O2. Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I. En la celda se producen reacciones de oxidación-reducción.
II. La celda produce agua como producto.
III. La celda produce principalmente energía térmica.
A) I y II
B) I y III
C) II y III
D) solo II
E) solo III
RESOLUCIÓN :
Analizamos las proposiciones.
I. Correcta
Se producen dos reacciones:
• oxidación del hidrógeno (combustible)
• reducción del oxígeno (comburente)
II. Correcta
El H2O es el único producto.
III. Incorrecta
La principal energía liberada es la eléctrica.
Rpta. : "A"
PREGUNTA 16 :
Respecto al 3-metil-1-butino, ¿cuáles de las siguientes proposiciones son correctas?
I. Tiene 11 enlaces sigma (σ).
II. Presenta 3 enlaces pi (𝛑).
III. No presenta isomería geométrica.
A) I y II
B) II y III
C) solo I
D) solo II
E) solo III
RESOLUCIÓN :
Analizamos cada proposición.
I. Incorrecta
La molécula presenta 12 enlaces sigma
II. Incorrecta
La molécula presenta 2 enlaces pi
III. Correcta
Isomería geométrica no es característica de los alquinos, sino de los alquenos y cicloalcanos.
Rpta. : "E"
PREGUNTA 17 :
Dada la siguiente tabla de constantes de ionización ácida a 25 ºC
¿Cuáles de las siguientes proposiciones son correctas?
I. Al HBrO le corresponde la base conjugada más estable.
II. HClO2 es el ácido más reactivo.
III. La base conjugada de HN3 es N^–3 y es la base conjugada más débil.
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 18 :
Dada la siguiente información de potenciales estándar de reducción, en voltios:
Indique la representación abreviada de la celda galvánica que puede construirse y que genere el mayor potencial (en voltios).
A) Ag(s) / Ag+(1 M) || Cu2+(1 M) / Cu(s)
B) Ag(s) / Ag+(1 M) || Ni2+(1 M) / Ni(s)
C) Cu(s) / Cu2+(1 M) || Ag+(1 M) / Ag(s)
D) Cu(s) / Cu2+(1 M) || Ni2+(1 M) / Ni(s)
E) Ni(s) / Ni2+(1 M) || Ag+(1 M) / Ag(s)
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 19 :
Se tiene una mezcla de tetróxido de dinitrógeno y de dióxido de nitrógeno en equilibrio, a 0 ºC y 1 atm, de acuerdo a la reacción
Si en esas condiciones la presión parcial del N2O4(g) es 0,8 atm, determine el valor de la constante Kc.
A) 2,2×10^– 3
B) 1,1×10^– 2
C) 5,0×10^– 2
D) 2,5×10^– 1
E) 5,0×10^– 1
RESOLUCIÓN :
Rpta. : "A"
PREGUNTA 20 :
Una solución preparada mezclando 5 g de tolueno, C7H8, con 225 g de benceno, C6H6, tiene una densidad de 0,976 g/mL. Calcule la molaridad del tolueno en dicha solución.
Masas molares (g/mol): tolueno=92; benceno=78
A) 0,05
B) 0,11
C) 0,15
D) 0,23
E) 0,26
RESOLUCIÓN :
Rpta. : "D"